(Desde Cambridge, Massachusetts, Estados Unidos) Es tiempo de graduaciones en la estimulante y hermosa ciudad de Cambridge, que combina con eclecticismo, lo clásico y lo moderno, rodeando en círculo a la ciudad de Boston, y alberga los dos claustros académicos más prestigiosos del mundo: la Universidad de Harvard y el MIT —el Instituto de Tecnología de Massachusetts—. De allí , saldrán los mejores científicos, investigadores y distintos eslabones de la ciencia y la tecnología globales. Desde allí nos proponen vivir más y mejor.
Esta base académica de excelencia, que tiene a Cambridge como nodo estratégico fundamental, explica por qué la industria farmacéutica, sobre todo la denominada big pharma, decidió instalarse ahí y diseñar ecosistemas científicos virtuosos con otras especialidades como la biotecnología, la tecnología, la biología computacional y la ciencia de datos, entre otras, necesarias para desarrollar nuevos tratamientos y terapias que incluyan al mayor número de personas posible.
Ser ágiles es lo que comprendieron las farmacéuticas tradicionales que necesitan para continuar creciendo consolidar esas alianzas con las biotecnológicas para crear la medicina del futuro. Aquí en Cambrigde se está diseñando lo que vendrá con la aplicación de las terapias génicas y las celulares, que permitirán tratar enfermedades cardiovasculares, neurodegenerativas, —ya reunió evidencia en Parkinson—, oncológicas —como cáncer de páncreas, de hígado—, y las genéticas o llamadas poco frecuentes, como la distrofia muscular de Duchenne y la atrofia muscular espinal, entre otras
Esta constelación de males son considerados de época porque evidencian un signo propio del siglo XXI, las sociedades más envejecidas. La población mundial, que no ha parado de crecer, alcanzó los 8.000 millones de personas a mediados de noviembre de 2022, y cuenta con una expectativa de vida que oscila entre los 75 y 85 años, aunque los promedios son muy desiguales entre los países. Viviremos más.
 El laboratorio global Bayer está tomando decisiones acorde a los tiempos. “La IA nos permitirá avanzar en los estudios más rápido, en la fase anterior a la pre clínica, ya incluimos un montón de IA por medio de la biología computacional” (Gettyimages)
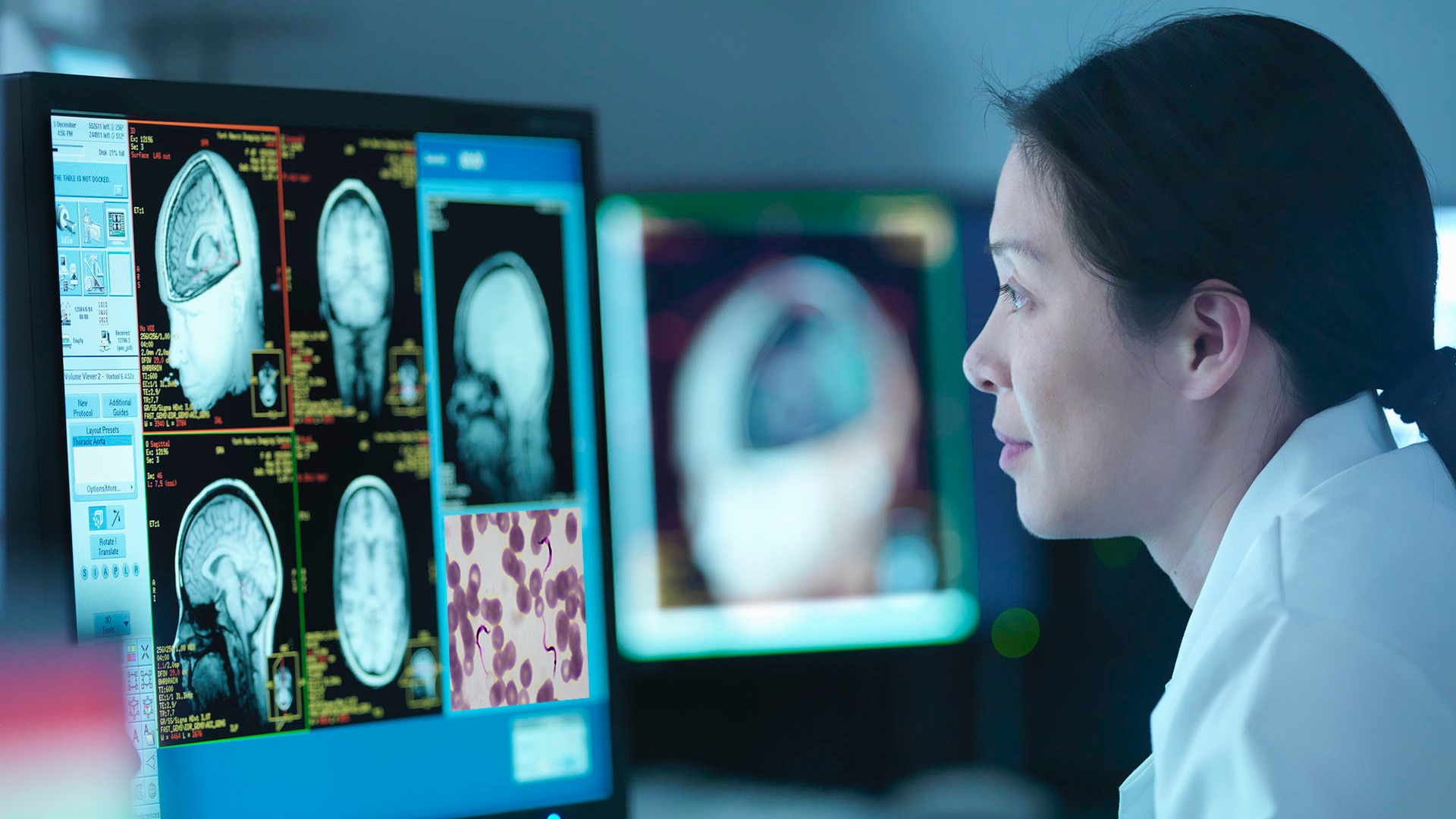
El laboratorio global Bayer está tomando decisiones acorde a los tiempos. “La IA nos permitirá avanzar en los estudios más rápido, en la fase anterior a la pre clínica, ya incluimos un montón de IA por medio de la biología computacional” (Gettyimages)Lejos de ciencia ficción, la científica Sandra T., es una de las líderes del vanguardista laboratorio biotecnológico BlueRock, en la ciudad de Cambridge y adquirido por Bayer en 2022. Allí guarda celosa y orgullosamente en sus ultrafreezers cajitas con células de personas sanas, y que además de estudiarlas dedicadamente, luego servirán para reparar y hasta reprogramar las células de pacientes enfermos de Parkinson, del corazón o de algún tipo de cáncer.
La técnica CRISPR —acrónimo en inglés de Clustered Regularly Interspaced Short Palindromic Repeats o Repeticiones Palindrómicas Cortas Agrupadas y Regularmente Espaciadas— emerge como tecnología dominante en ese tipo de terapias. Actúan como si fueran “tijeras moleculares” que, bajo estrictos criterios científicos, éticos y de seguridad, ayudarán a reparar ADN enfermo. La tecnología CRISPR puede ofrecer la capacidad de modificar o corregir directamente los cambios asociados a una enfermedad subyacente en el genoma y reescribir así la ciencia y la medicina actual
Esta imagen de la doctora Sandra T., sirve para cimentar la idea de que una big pharma ya no puede sola, sino que necesita establecer alianzas virtuosas con organizaciones biotecnológicas y tecnológicas con el objetivo de crear la ciencia del futuro.
En el campo de la terapia celular y génica, los resultados positivos de los estudios clínicos también ofrecen una ventaja potencial para las big pharma y así lo entendió el gigante de origen alemán Bayer, que busca constantemente nuevas miradas en el ecosistema biotecnológico.
Ante esto, complementar la experiencia interna con colaboraciones externas sigue siendo una parte vital de la estrategia para expandir su experiencia en I+D y desarrollar terapias innovadoras, como ocurre con las compras de los hubs biotech BlueRock y AskBio.
 De sus dos claustros académicos, de los más prestigiosos del mundo: la Universidad de Harvard y el MIT —el Instituto de Tecnología de Massachusetts—, saldrán los mejores científicos y eslabones de la ciencia y la tecnología del mundo. Desde allí nos proponen vivir más y mejor
De sus dos claustros académicos, de los más prestigiosos del mundo: la Universidad de Harvard y el MIT —el Instituto de Tecnología de Massachusetts—, saldrán los mejores científicos y eslabones de la ciencia y la tecnología del mundo. Desde allí nos proponen vivir más y mejorBlueRock: las terapias génicas por dentro
BlueRock es pionera en terapias con células madre y, hoy está desarrollando una línea creciente de tratamientos innovadores para pacientes con enfermedades neurológicas, inmunológicas, cardiovasculares y oftalmológicas. Su programa más avanzado se dedica al tratamiento de la enfermedad de Parkinson. Según la Fundación Parkinson, más de 10 millones de personas padecen esta enfermedad en el mundo.
Dentro del futurismo que propone —incluso el edificio— el presidente y director ejecutivo de BlueRock Therapeutics, Seth Ettenberg, resumió a Infobae el trabajo de innovación y el enorme objetivo de este hub científico.
“Para hablar de una terapia celular, hay que comprender primero qué es una Célula Madre Pluripotente Inducida (IPSC, por sus siglas en inglés). Voy a simplificarlo así: en el desarrollo hay un punto en nuestro ciclo de vida en el que existimos como cuatro células o dos células. En ese momento, esa célula se llama pluripotente, lo que significa que puede dar origen a cualquier tipo de célula en el cuerpo. Puede convertirse en cabello, piel, hueso, músculo, ese tipo de células es con las que trabajamos. Ahora bien, las células madre pluripotentes son fenomenales porque pueden convertirse en cualquier célula del cuerpo”, aseguró Ettenberg.
Y destacó un punto que consideró aún “más importante y relevante para el trabajo que hace BlueRock”, la investigación de las llamadas “células pluripotentes inducidas”. Continuó su explicación: “esto significa que, a partir de un donante sano, tomamos una muestra de sangre y luego reprogramamos esa célula. Esto es la ciencia fundacional que se llevó un Premio Nobel gracias a (Shinya) Yamanaka, de Japón, que en 2012 ganó el Premio Nobel de Fisiología y Medicina, lo cual es asombroso considerando dónde estamos hoy en día. Reprogramamos esa célula para que se convierta en lo que llamamos un lienzo en blanco”.
 Seth Ettenberg, presidente y director ejecutivo de BlueRock Therapeutics: «En BlueRock, en nuestra alianza con Bayer, aprendimos cómo hacer investigación académica y luego cómo traducirlo desde el banco de pruebas y cómo industrializar ese proceso»
Seth Ettenberg, presidente y director ejecutivo de BlueRock Therapeutics: «En BlueRock, en nuestra alianza con Bayer, aprendimos cómo hacer investigación académica y luego cómo traducirlo desde el banco de pruebas y cómo industrializar ese proceso»De esta forma, y en asociación con la Universidad de Salud Pública de Harvard, BlueRock está desarrollando ensayos clínicos para el tratamiento del Parkinson con la revolucionaria técnica explicada por Ettenberg: son neuronas dopaminérgicas derivadas de células madre pluripotentes que se implantan en el cerebro y se dirigen a la causa raíz de la enfermedad.
Se trata de su programa más avanzado, BRT-DA01, que ya ha completado la inscripción en el ensayo clínico de Fase I en 12 pacientes y se espera que la lectura de datos se realice en la segunda mitad de 2023.
AskBio y el “delivery” de genes
Por su parte, AskBio (Asklepios BioPharmaceutical) también fue adquirida por Bayer AG desde fines de 2020 y actúa en forma independiente en la investigación de terapias celulares y génicas, buscando avances en la tecnología aplicada a este segmento con el fin de erradicar las enfermedades genéticas o raras. Desde 2001, AskBio se encuentra en una búsqueda incansable por avanzar en esa tecnología y en esas terapias. La cartera clínica de la organización abarca una amplia gama de trastornos del sistema nervioso central, neuromusculares, metabólicos y cardiovasculares.
Tiene su sede en Research Triangle Park, Carolina del Norte, un centro de biotecnología disruptivo con casi 600 empresas de ciencias de la vida, y cuenta con instalaciones adicionales de investigación y desarrollo en Edimburgo, Escocia, y París, Francia, además de España.
Actualmente, la compañía está avanzando en varios candidatos preclínicos y seis se encuentran en estadio clínico, abordando soluciones para las enfermedades de Parkinson, Pompe y Huntington, además de estar desarrollando una terapia génica como un nuevo enfoque potencial para el tratamiento de la insuficiencia cardíaca congestiva.
 El Boston-Cambridge Innovation Campus (BRIC): fueron invertidos USD 140 millones de dólares en la construcción del campus que tiene como objetivo la investigación oncológica molecular y de precisión para el desarrollo de nuevas terapias contra el cáncer. (Gentileza Bayer)
El Boston-Cambridge Innovation Campus (BRIC): fueron invertidos USD 140 millones de dólares en la construcción del campus que tiene como objetivo la investigación oncológica molecular y de precisión para el desarrollo de nuevas terapias contra el cáncer. (Gentileza Bayer)“Los cambios de fondo en la búsqueda primero del tratamiento para las enfermedades más prevalentes que aglutinan las mayor cantidad de muertes en el mundo, con las cardiológicas y oncológicas, son las que lideran la lista, no puede hacerse en la soledad de un único ‘momento ¡eureka!’. Es necesario poner en marcha un ecosistema virtuoso entre hubs tecnológicos, industria techie con la IA como punta de lanza y el eslabón de las instituciones académicas”, aseguró Daniel Londero, presidente de la División farmacéutica de Bayer para el Conosur.
Respecto de este último punto, precisó que “la IA nos permitirá avanzar en los estudios más rápido, en la fase anterior a la pre clínica, ya incluimos un montón de IA por medio de la biología computacional”.
Sin que le tiemble la voz, el director de Terapia Génica de AskBio, MD Roger Hajjar, explicó a Infobae: “Ya hacemos ‘delivery’ de genes” en pacientes con afecciones cardíacas y para quienes la enfermedad va y viene. Es decir, luego de un infarto o un ACV, el corazón no sigue funcionando bien y una terapia génica puede ser la diferencia”. Esta terapia llega a subsanar lo que ocurre con “algunas enfermedades, sobre todo las genéticas, a veces llamadas poco frecuentes, en las que existe la odisea diagnóstica. Por eso, el paciente llega a una terapia génica luego de muchos fracasos alrededor de su enfermedad, en su tratamiento”.
BlueRock y las bases de su ciencia
El siguiente es parte del diálogo que Infobae mantuvo con el científico Ettenberg en la sede de BlueRock, hub que él lidera.
—¿En qué se basa el trabajo que desarrollan junto a Bayer?
—En BlueRock, en nuestra alianza con Bayer, aprendimos cómo hacer investigación académica y luego cómo traducirlo desde el banco de pruebas y cómo industrializar ese proceso. Poder ser ágiles y cambiar muy rápidamente, en lugar de estar en una multinacional muy grande y tener un tiempo de reacción más lento. Y así es como podemos operar todos los días, pero operamos como cualquier otra empresa de biotecnología que puedes encontrar aquí en Cambridge.
 BlueRock es pionera en terapias con células madre y, en colaboración con Bayer, está desarrollando una línea creciente de tratamientos innovadores para pacientes con enfermedades neurológicas, inmunológicas, cardiovasculares y oftalmológicas (Getty)
BlueRock es pionera en terapias con células madre y, en colaboración con Bayer, está desarrollando una línea creciente de tratamientos innovadores para pacientes con enfermedades neurológicas, inmunológicas, cardiovasculares y oftalmológicas (Getty)—¿Qué detalles puede darnos respecto de los estudios de BlueRock sobre Parkinson?
—Aquí en BlueRock pensamos en las enfermedades humanas en las que la pérdida de la célula fundamental conduce a la patología que observamos. Y no hay un mejor ejemplo de esto que el Parkinson. Sabemos por muchas décadas de investigación que, desde el primer diagnóstico de Parkinson, como paciente has perdido más del 50% de lo que se llaman neuronas dopaminérgicas en el estriado de tu cerebro. Y lo que sucede con el tiempo, es que tenemos medicamentos muy buenos en el estándar de atención llamados levodopa, (NdeR: la levodopa pertenece a una clase de medicamentos llamados agentes del sistema nervioso central. Su acción consiste en convertirse en dopamina en el cerebro) que es la base, la dopamina, que no ha cambiado en los últimos 60 años.
Y tanto los médicos como los pacientes saben que, desde que recibes el diagnóstico tienes un momento de “luna de miel”, lo que llaman un período de buenos efectos de la levodopa, pero con el tiempo te deterioras.
Los beneficios del medicamento desaparecerán y perderás cada vez más funcionalidad y eso se debe a la pérdida de más y más de esas neuronas dopaminérgicas en tu cerebro. Entonces, ese “buscar y reemplazar” es muy simple, elegante y hermoso en su concepto. Encontramos enfermedades como esa y reemplazamos la célula que se perdió debido a esa enfermedad para devolverle plena funcionalidad al paciente. Pero por elegante y hermoso que sea, técnicamente es muy audaz intentar esto. Nadie lo ha hecho antes y solo puedes imaginar cómo es entregar las células al lugar correcto, hacer que se injerten en el cuerpo, se integren y se conviertan en parte de esa red neural.
 «Mientras hablamos de esto y escuchas sobre la terapia celular, ya hay algunas terapias celulares en el mercado. De hecho, en oncología, hay productos que se están vendiendo en el mercado», dijo Ettenberg (Gettyimages)
«Mientras hablamos de esto y escuchas sobre la terapia celular, ya hay algunas terapias celulares en el mercado. De hecho, en oncología, hay productos que se están vendiendo en el mercado», dijo Ettenberg (Gettyimages)Encontramos y reemplazamos, restauramos la función y, por lo tanto, revertimos la enfermedad. A menudo escucharás referirnos como medicina regenerativa, reconstruyendo los tejidos esenciales. El segundo elemento de nuestra cartera, y en el futuro escucharás cada vez más sobre esto y ya lo estás escuchando de otras compañías, es la capacidad de ingeniería del genoma.
—¿Por qué la base de este tratamiento es lo que llaman célula madre pluripotente?
—Ahora podemos, a partir de nuestra célula madre pluripotente, crear cualquier tipo de célula en el cuerpo y luego cambiar cualquier gen dentro del genoma de esa célula para crear una célula que tenga una mejor aplicación terapéutica, donde sepamos de la existencia de un medicamento o una proteína adicionales o una enzima. También hemos escuchado recientemente sobre la idea de enfermedades ultrararas donde puede faltar una enzima. Podemos incorporar eso en nuestro tipo de célula y entregar esa enzima al lugar adecuado para ese paciente.
—¿En que terapia celular alogénica que están desarrollando en BlueRock?
—Mientras hablamos de esto y escuchas sobre la terapia celular, ya hay algunas terapias celulares en el mercado. De hecho, en oncología, hay productos que se están vendiendo en el mercado. Lo que quiero que entiendas sobre ellos es que se llaman autólogos, lo que significa que tomo una célula tuya, hago algo con ella en el laboratorio y la vuelvo a poner en ti para que tu cuerpo no la rechace. Es como lo que se hace con un injerto de tejido.
 Desde 2001, AskBio se encuentra en una búsqueda incansable por avanzar en esa tecnología y en esas terapias
Desde 2001, AskBio se encuentra en una búsqueda incansable por avanzar en esa tecnología y en esas terapiasEso es muy diferente de lo que te voy a contar, que es la terapia celular alogénica, que acabo de comenzar a describirte. Tomo una célula de un donante sano, hago algo con ella en el laboratorio, pero luego puedo hacer lotes escalables indefinidos. Puedo hacer que esto sea más parecido a lo que entendemos como un medicamento, pero que cualquier clínica y paciente pueda entender la calidad, los beneficios y los riesgos de ese medicamento.
Así que hay una gran ventaja en poder hacer esto, pero es un poco no probado. Y ahí es exactamente donde nos encontramos. BlueRock existe en el límite de lo que es posible científicamente y lo que es técnicamente desafiante de hacer. Cuando miras el pipeline de BlueRock, en realidad es bastante amplio en cuatro áreas de enfermedades y hay varios tipos de células dentro de esas áreas. Cada uno de estos tipos de células es una hermosa obra maestra en sí misma al intentar crearla. Y lo que quiero que pienses es esa misma hipótesis con la que comencé, encontrar y reemplazar.
—¿Qué detalles me puede dar sobre la aplicación de estas innovadoras terapias en el área de la cardiología?
—La insuficiencia cardíaca es una de las principales causas de muerte entre nuestra población. Tienes un infarto isquémico, un evento, que conduce a la pérdida de sangre de esas células. Esa pérdida de sangre realmente mata esas células. Entonces, en la práctica de la medicina durante los últimos 100 años ponemos medicamentos y fármacos en esas células muertas, deseando que vuelvan a la vida. Lo que hacemos en BlueRock Therapeutics es fabricar esos mismos miocitos cardíacos y luego injertarlos en el paciente. Es técnicamente difícil, pero hacia eso nos dirigimos, porque si podemos hacer eso, podemos traer y restaurar la funcionalidad completa a ese corazón, al menos en el injerto ECMO. Y puedes pensar en esa misma hipótesis exacta mientras miras. Nuestro proyecto más avanzado en el que estamos trabajando se llama Bemdinapraso, que ahora está completamente inscrito en un ensayo clínico de Fase I.
 Adib Jacob, presidente de la División Farmacéutica de Bayer para Brasil y América Latina: «Bayer está intentando ver los dilemas de la humanidad en los próximos 20 a 30 años»
Adib Jacob, presidente de la División Farmacéutica de Bayer para Brasil y América Latina: «Bayer está intentando ver los dilemas de la humanidad en los próximos 20 a 30 años»—¿Cómo están logrando algo tan extremadamente desafiante?
Lo primero en lo que debemos pensar es en la investigación y el desarrollo. Esto es parte de cualquier empresa biotecnológica. Debes comprender la ciencia, debes comprender qué tipo de medicamento estás creando y cómo se relaciona con esa enfermedad, y luego debes llevarlo a través de pruebas clínicas para demostrar tanto la seguridad como la eficacia. Además de eso, la fabricación aquí es diferente a la fabricación en casi cualquier otro producto farmacéutico que puedas imaginar.
Estamos produciendo medicamentos dopaminérgicos a escala para muchas personas al mismo tiempo. Nunca se ha hecho antes, y la forma en que lo hacemos y cómo interactuamos con los reguladores, la calidad y las características que utilizamos son muy diferentes
La medicina preventiva y la detección temprana
En esta nueva era hay conceptos que llegaron para quedarse “medicina preventiva” y “detección temprana” son la clave de la transformación en el ámbito de la salud global.
El doctor Londero, como presidente de la División Farmacéutica de Bayer para el Conosur, lo explicó a Infobae de esta forma: “Bayer establece esa conversación con los pacientes y asociaciones de pacientes. Trabajamos para educar y concientizar. Por ejemplo, con la droga Firenenona nos ocupamos de hablar con los médicos que atienden a esos pacientes con diabetes para ayudarlos a que ese paciente no llegue a la falla renal y así evitar llegar a la falla renal, a la diálisis. Podemos prevenir eso hablando con los médicos y las asociaciones de pacientes”.
 «La insuficiencia cardíaca es una de las principales causas de muerte entre nuestra población. Tienes un infarto isquémico, un evento, que conduce a la pérdida de sangre de esas células. Esa pérdida de sangre realmente mata esas células», dijo Ettenberg (Getty)
«La insuficiencia cardíaca es una de las principales causas de muerte entre nuestra población. Tienes un infarto isquémico, un evento, que conduce a la pérdida de sangre de esas células. Esa pérdida de sangre realmente mata esas células», dijo Ettenberg (Getty)Tanto es así, agregó, que “la mayoría de la inversión de Bayer tiene que ver con educar a las asociaciones científicas. Cuando nosotros lanzamos estos productos, que generan una nueva forma de atención, tenemos que trabajar con el médico, que no estaba acostumbrado a esa prevención y con los pacientes. El 90% de nuestro trabajo es educación”.
El presidente de la División Farmacéutica de Bayer para Brasil y América Latina, Adib Jacob, sumó, por su parte, que “además de fortalecer la medicina de prevención, hasta ahora tratábamos de prevenir, pero tenemos muchos pacientes crónicos. El gran objetivo de la big pharma es curar enfermedades genéticas, el cáncer, y revertir enfermedades autoinmunes en alianza con biotecnológicas”.
—¿Cómo vislumbra el futuro de una big pharma con Bayer?
—Adib Jacob: Bayer está intentando ver los dilemas de la humanidad en los próximos 20 a 30 años. Personas viviendo mucho más en centros urbanos, hábitos de alimentación, sedentarismo. Y ahí se tiene una visión que, por ejemplo, las enfermedades del corazón, metabólicas, serán muy importantes en los próximos 20, 30 años, también el cáncer. Si se vive más, hay mucho más riesgo de un tumor y también de enfermedades neurodegenerativas, que igualmente están muy conectadas con la edad. Hoy una pharma no puede hacer todo sola, tiene que concentrar el conocimiento Por eso seleccionamos áreas terapéuticas donde tenemos ya conocimiento y agregamos conocimiento con los hubs biotecnologicos como BlueRock y AskBio, entre otras.
 Daniel Londero, Presidente de la División Farmacéutica de Bayer para Conosur: “Los cambios de fondo en la búsqueda de la cura para las enfermedades más prevalentes que aglutinan las mayor cantidad de muertes en el mundo, con las cardiológicas y oncológicas que lideran la lista, no puede hacerse en la soledad de un único ‘momento ¡eureka!’»
Daniel Londero, Presidente de la División Farmacéutica de Bayer para Conosur: “Los cambios de fondo en la búsqueda de la cura para las enfermedades más prevalentes que aglutinan las mayor cantidad de muertes en el mundo, con las cardiológicas y oncológicas que lideran la lista, no puede hacerse en la soledad de un único ‘momento ¡eureka!’»Londero destacó que, “si llegamos a una cura del Parkinson vamos a disminuir mucho el costo del sistema de salud, por las consultas, más la internación de gente joven que no trabaja”. “Vamos a sacar una terapia para curar el Parkinson”, afirmó Adib Jacob con absoluta seguridad. Eso permitirá que la persona “esté de vuelta en la sociedad”, pero advirtió que “para esto hay que sensibilizar a los pagadores del costo del sistema de la necesidad de una terapia génica, de una cura. En segundo lugar debe haber financiamiento y en tercer lugar, modelos de risk sharing. Por ejemplo, si el producto no funciona, no habría, por ejemplo, que pagar. Debe haber camaradería entre pagadores y la industria. Es otro modelo logístico, porque es terapia individualizada, es otro modelo regulatorio. Las agencias están empezando a discutir cómo lo aprobamos. Es otro paradigma”, concluyó.
Infobae







